Hóa trị là một trong những phần bắt buộc bạn phải nhớ khi học hóa. Vì vậy, Trung tâm WElearn gia sư đã tổng hợp lại cho bạn tất cả những thông tin liên quan đến hóa trị, đặc biệt là bảng hóa trị lớp 8. Cùng theo dõi để nắm chắc kiến thức hóa học của mình hơn nhé!
Hóa trị là gì?
Hóa trị là số lượng liên kết hóa học mà một nguyên tử có thể hình thành với các nguyên tử khác. Nó được xác định bằng số electron mà một nguyên tử có thể mất, nhận hoặc chia sẻ để đạt được cấu hình electron bền vững (thường là cấu hình của khí hiếm gần nhất).
Hóa trị của nguyên tố trong hợp chất ion được gọi là điện hóa trị, có giá trị bằng với điện tích của ion tạo thành từ nguyên tố đó.
Cách xác định hoá trị
Hóa trị của các nguyên tố được xác định theo hóa trị hóa trị đơn vị của nguyên tố Hidro (mặc định là hóa trị 1) và hóa trị của nguyên tố Oxi (mặc định là hóa trị 2).
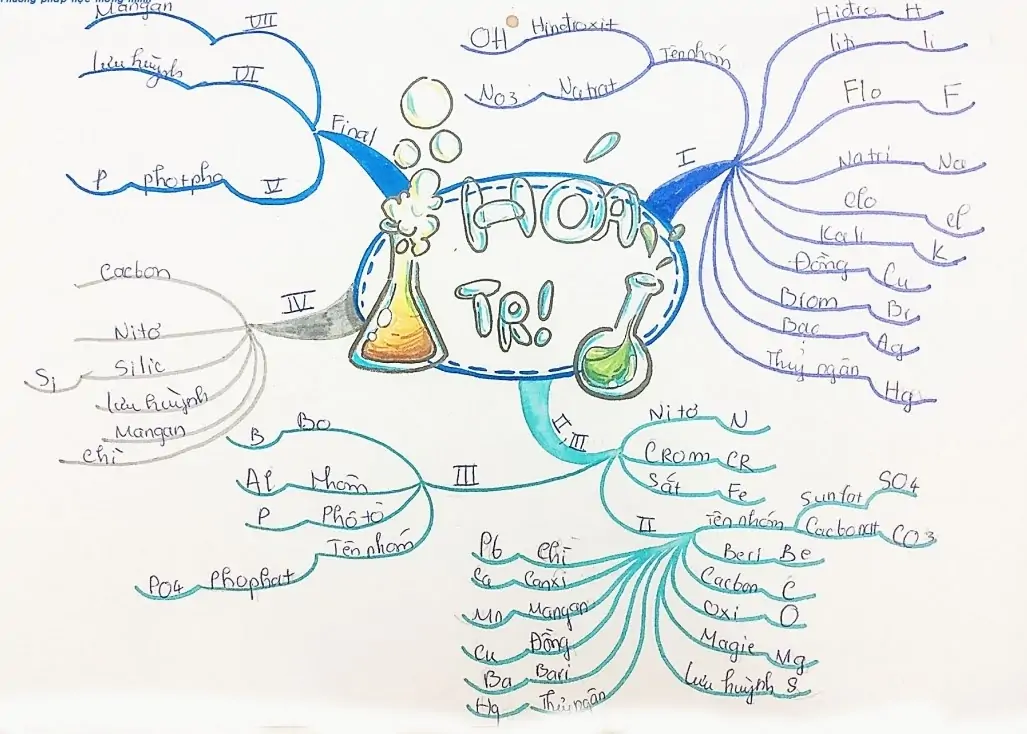
Bảng hóa trị các nguyên tố hóa học lớp 8 đầy đủ nhất
Hóa trị của nguyên tử
| Số proton | Tên Nguyên tố | Ký hiệu | Hoá trị |
| 1 | Hiđro | H | I |
| 2 | Heli | He | |
| 3 | Liti | Li | I |
| 4 | Beri | Be | II |
| 5 | Bo | B | III |
| 6 | Cacbon | C | IV, II |
| 7 | Nitơ | N | II, III, IV… |
| 8 | Oxi | O | II |
| 9 | Flo | F | I |
| 10 | Neon | Ne | |
| 11 | Natri | Na | I |
| 12 | Magie | Mg | II |
| 13 | Nhôm | Al | III |
| 14 | Silic | Si | IV |
| 15 | Photpho | P | III, V |
| 16 | Lưu huỳnh | S | II, IV, VI |
| 17 | Clo | Cl | I,… |
| 18 | Argon | Ar | |
| 19 | Kali | K | I |
| 20 | Canxi | Ca | II |
| 24 | Crom | Cr | II, III |
| 25 | Mangan | Mn | II, IV, VII… |
| 26 | Sắt | Fe | II, III |
| 29 | Đồng | Cu | I, II |
| 30 | Kẽm | Zn | II |
| 35 | Brom | Br | I… |
| 47 | Bạc | Ag | I |
| 56 | Bari | Ba | II |
| 80 | Thuỷ ngân | Hg | I, II |
| 82 | Chì | Pb | II, IV |
Hóa trị của nhóm nguyên tử
| Tên nhóm | Hoá trị | Gốc axit | Axit tương ứng | Tính axit |
| Hiđroxit(*) (OH); Nitrat (NO3); Clorua (Cl) | I | NO3 | HNO3 | Mạnh |
| Sunfat (SO4); Cacbonat (CO3) | II | SO4 | H2SO4 | Mạnh |
| Photphat (PO4) | III | Cl | HCl | Mạnh |
| (*): Tên này dùng trong các hợp chất với kim loại. | PO4 | H3PO4 | Trung bình | |
| CO3 | H2CO3 | Rất yếu (không tồn tại) | ||
Cách học bảng hóa trị lớp 8 nhanh thuộc
Kali, Iot, Hiđro
Natri với Bạc, Clo một loài
Có hóa trị I bạn ơi
Nhớ ghi cho rõ kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cũng gần Bari
Cuối cùng thêm chú Oxi
Hóa trị II ấy có gì khó khăn
Bác Nhôm hóa trị III lần

Ghi sâu trí nhớ khi cần có ngay
Cacbon, Silic này đây
Là hóa trị IV không ngày nào quên
Sắt kia kể cũng quen tên
II, III lên xuống thật phiền lắm thay
Nitơ rắc rối nhất đời
I, II, III, IV khi thì là V
Lưu huỳnh lắm lúc chơi khăm
Lúc II, lúc VI khi nằm thứ IV
Photpho nói tới không dư
Nếu ai hỏi đến thì ừ rằng V
Bạn ơi cố gắng học chăm
Bài ca hóa trị suốt năm rất cần
Quy tắc hóa trị cần nhớ
Quy tắc hóa trị được phát biểu như sau: “Trong phân tử có công thức hóa học xác định: tích của chỉ số và hóa trị của nguyên tố này bằng tích của chỉ số và hóa trị của nguyên tố kia.”
Nghĩa là, với công thức hóa học AxBy (A có hóa trị là a và B có hóa trị là B). Ta có: x.a = y.b
Vì vậy, khi ta biết được 3 trong 4 số trong công thức trên, ta có thể tìm được giá trị còn lại.
Chuyển thành tỉ lệ: x/y = b/a
Trong trường hợp chỉ biết được 2 trong 4 giá trị trên, ta lấy x = b (hoặc b’) và y = a (hoặc a’). Nếu a’, b’ là những số nguyên đơn giản hơn so với a, b.
Khi đó AxBy là công thức đơn giản nhất.
Bài tập vận dụng về Hóa Trị
Bài tập 1: Tính hóa trị của các nguyên tố
a) Nhôm trong hợp chất Al2O3
b) Sắt trong hợp chất FeO
c) Crom trong hợp chất CrO và Cr2O3
Đáp án hướng dẫn giải chi tiết
a) Nhôm trong hợp chất Al2O3
Gọi hóa trị của nhôm trong hợp chất là x:
Ta có hóa trị của O (II)
Theo quy tắc hóa trị.
x = 3.II => x = 3 (III) . Vậy Nhôm có hóa trị bằng III trong hợp chất Al2O3
Tương tự làm với câu b); c)
Sắt trong hợp chất FeO có hóa trị là II
Crom trong hợp chất CrO và Cr2O3 có hóa trị lần lượt là II và III
Bài tập 2. Dựa vào hóa trị các nguyên tố. Cho biết công thức hóa học nào viết sai, công thức hóa học nào viết đúng: MgCl, NaO, BaO, NaCl, AlO3, K2O, Fe2O3
Đáp án hướng dẫn giải chi tiết
MgCl, NaO, BaO, NaCl, AlO3, K2O, Fe2O3
Công thức viết đúng là: BaO, K2O, Fe2O3
Công thức viết sai là: MgCl (MgCl2); NaO (Na2O); AlO3 (Al2O3)
Bài tập 3. Lập công thức hóa học của các hợp chất sau:
a) C (IV) và S (II)
b) Fe (II) và O.
Đáp án hướng dẫn giải chi tiết
a) Bước 1: Công thức hóa học của C (IV) và S (II) có dạng
Bước 2: Biểu thức quy tắc hóa trị: x.IV = y.II
Chuyển thành tỉ lệ:
Bước 3: Công thức hóa học cần tìm là: CS2
b) Công thức hóa học của Fe(III) và O có dạng:
Biểu thức quy tắc hóa trị: x.III = y.II
Chuyển thành tỉ lệ:
Chọn x = 2, y = 3
Công thức hóa học cần tìm là: Fe2O3
Như vậy, WElearn đã tổng hợp Tất Tần Tật Về Bảng Hóa Trị lớp 8. Hy vọng những kiến thức mà bài viết chia sẻ có thể giúp bạn học tốt môn Hóa học hơn. Chúc bạn thành công nhé!
Nếu bạn đang phân vân giữa việc chọn gia sư dạy Hóa tại nhà hay học hóa tại trung tâm, hãy cân nhắc kỹ lưỡng về ưu điểm và nhược điểm của mỗi phương pháp. Việc học tại nhà với gia sư sẽ giúp các em tiết kiệm thời gian và công sức đi lại. Các em không cần phải di chuyển đến trung tâm, mà gia sư sẽ đến tận nhà để dạy theo lịch rảnh của các em. Điều này giúp các em có thể tận dụng thời gian học tập một cách hiệu quả hơn. Với hình thức dạy kèm 1-1, các em sẽ được học theo nhu cầu riêng của mình. Gia sư có thể tập trung vào những khái niệm hoặc bài tập mà các em cảm thấy khó khăn, giúp các em hiểu rõ hơn và nắm vững kiến thức của từng nội dung bài học.
Trung tâm gia sư WElearn tự hào là địa chỉ tin cậy cung cấp gia sư Hóa văn hàng đầu cho các em học sinh và quý phụ huynh. Hãy gọi ngay cho WElearn để đặt lịch hẹn với gia sư miễn phí!
- Hotline: 0906782291
- Facebook: https://www.facebook.com/welearngiasu
- Gmail: welearnvietnam@gmail.com
- Website: https://welearnvn.com/
